eISSN 2444-7986
DOI: https://doi.org/10.14201/orl.22759
ARTÍCULO ORIGINAL
DISEÑO, MODELADO 3D Y OPTIMIZACIÓN DEL COMPORTAMIENTO MECANOACÚSTICO DE UN NUEVO TUBO DE VENTILACIÓN TRANSTIMPÁNICO
Design, 3D modeling and mechanoacoustical behaviour optimization of a new ventilation tube
Luis A. VALLEJO-VALDEZATE1; Angélica BRAGADO2; Antonio HIDALGO-OTAMENDI2;3;
Elisa GIL-CARCEDO1; David HERRERO-CALVO1; Sara FERNÁNDEZ-CASCÓN1
1Servicio de Otorrinolaringología. Hospital Universitario Río Hortega. Universidad de Valladolid. Valladolid. España.
2Centro para la Investigación y el Desarrollo de la Automoción (CIDAUT). Valladolid. España.
3Centro para el Estudio y Control del Ruido (CECOR). Valladolid. España.
Correspondencia: lvallejovaldez@movistar.es
Fecha de recepción: 24 de marzo de 2020
Fecha de aceptación: 9 de abril de 2020
Fecha de publicación: 10 de abril de 2020
Fecha de publicación del fascículo: 1 de diciembre de 2020
Conflicto de intereses: Los autores declaran no tener conflictos de intereses
Imágenes: Los autores declaran haber obtenido las imágenes con el permiso de los pacientes
Política de derechos y autoarchivo: se permite el autoarchivo de la versión post-print (SHERPA/RoMEO)
Licencia CC BY-NC-ND. Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional
Universidad de Salamanca. Su comercialización está sujeta al permiso del editor
RESUMEN: Introducción y Objetivos: En este trabajo mostramos un nuevo tubo de ventilación transtimpánico cuyo diseño pretende solventar los efectos indeseables aparecidos durante la inserción de tubos de ventilación actualmente comercializados; analizamos su comportamiento mecánico en un modelo 3D del oído a fin de optimizar su comportamiento acústico. Métodos: Para el diseño del tubo se empleó un software autoCAD; El comportamiento mecánico se analizó en un modelo computadorizado dinámico 3D del oído humano basado en el método de los elementos finitos (FEM). Resultados: El nuevo tubo de ventilación posee un tamaño y una masa significativamente menores a los actualmente disponibles en el mercado lo que provoca un menor interferencia en la vibración del sistema tímpano-osicular; su diseño facilita que permanezca insertado mientras las condiciones del paciente así lo aconsejen evitando su caída hacia la caja o su precoz extrusión. Conclusiones: Las ventajas teóricas biológicas y acústicas del nuevo tubo desarrollado (con menor masa y cuyo diseño evita las complicaciones de los actuales) puede abrir una nueva posibilidad de tratamiento de la otitis media seromucosa crónica.
PALABRAS CLAVE: tubo de ventilación transtimpánico; tubo de timpanotomía; otitis seromucosa; otitis con derrame.
SUMMARY: Introduction and Objetive: We show a new trans-tympanic ventilation tube whose design and mass are intended to solve the undesirable effects that appeared during the insertion of currently commercialized ventilation tubes; We analyze its mechanical behavior in a 3D model of the ear in order to optimize its acoustic behavior. Methods: For the design of the tube an autoCAD software was used; The mechanical behavior was analyzed in a 3D dynamic computerized model of the human ear based on the finite element method (FEM). Results: The new ventilation tube has a size and mass significantly smaller than those currently available in the market, which causes less interference in the vibration of the eardrumosicular system; Its design facilitates it to remain inserted while the patient’s conditions so advise avoiding its fall into the middle ear cavity or its early extrusion. Conclusions: The biological and acoustic advantages of the new developed tube (with less mass and whose design avoids the complications of the current ones) can open a new possibility of treatment of chronic seromucous otitis media.
KEYWORDS: Transtympanic ventilation tube; Tympanostomy Tube; Grommet; Otitis media with effusion; Seromucous otitis.
Los genéricamente denominados tubos de ventilación transtimpánicos (también llamados aireadores, diábolos, drenajes transtimpánicos, tubos de miringostomía o tubos de equipresión) son pequeñas prótesis utilizadas para suplir la función de la trompa de Eustaquio por algún motivo disfuncionante. Su implantación constituye una de las intervenciones más frecuentes en la infancia, no siendo excepcional en el adulto.
Existe un gran número de diseños de estos tubos en función de las preferencias del cirujano que les desarrolló, pero a pesar de esta variedad de formas, materiales y tamaños, presentan deficiencias; que están en el origen de complicaciones o efectos indeseados asociados a la inserción de los tubos de miringostomía (Figura 1). Se ha descrito la caída de estos tubos hacia la caja timpánica, su sobreinfección, la formación de granulaciones timpánicas, la alteración en la migración epitelio timpánica con posibilidad de desarrollo de colesteatoma, la presencia de daños permanentes en la membrana timpánica (timpanosclerosis, perforación residual, membrana monomérica en la zona de inserción), obstrucción. Otras deficiencias debidas a su diseño son la falta de control del proceso de eliminación del tubo lo que hace frecuente la necesidad de implantarles repetidamente al no haberse resuelto aún las causas de la disfunción tubárica en el momento de la extensión del tubo.
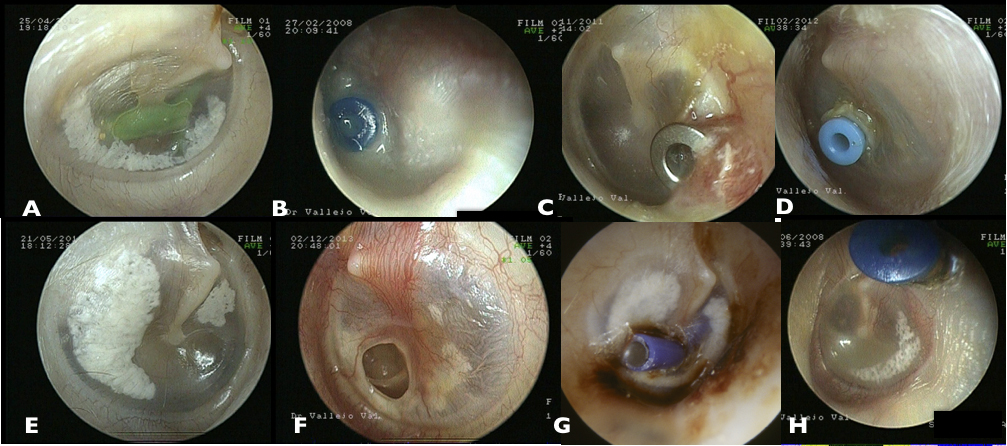
Figura 1. Algunas complicaciones habituales asociadas al uso de tubos de miringostomía: Caída hacia la caja timpánica (a), sobreinfección (b), formación de granulomas timpánicos (c), alteración de la migración epitelial (d), formación de placas de timpanosclerosis (e), perforación residual (f), oclusión mucosa (g) y desprendimiento prematuro (h).
Salvo algún diseño de tubo relativamente reciente [1] o el intento de fabricarles con material reabsorbible [2,3] (lo que, al igual que la falta de control del proceso de eliminación de los tubos convencionales, es más una deficiencia que una ventaja) la mayor parte de los diseños de los tubos de ventilación actualmente en uso se llevaron a cabo a mediados del pasado siglo por prestigiosos otólogos de la época (Shea, Paparella, Goode) no habiéndose diseñado desde entonces ningún tubo que tenga en cuenta las deficiencias clínicas que presentan los actuales ni la interferencia del mismo en las características mecánicas del oído medio.
Crysdale [4], tras comparar varios tipos de estos tubos, estableció una serie de características que, en su criterio, debería cumplir el tubo de ventilación ideal:
1. Habría de ser rápida y fácilmente implantable por la mayor parte de los otorrinolaringólogos
2. Su diseño debería impedir su caída hacia el oído medio.
3. Habría de ser capaz de ventilar el oído medio mientras permaneciese insertado en el tímpano impidiendo, a su vez la entrada de agua o suciedad en el oído medio
4. Su diseño debería dificultar su rápida extrusión y a la vez permitir su retirada sin dificultad
5. El diseño del tubo y el material con el que se fabricase no deberían provocar daños permanentes en el oído medio o en la membrana timpánica que originasen mermas en la capacidad auditiva.
En el presente trabajo presentamos el diseño de un nuevo tubo transtimpánico que intenta respetar los criterios de idoneidad biológica de Crysdale y analiza su comportamiento mecánico a fin de optimizar sus propiedades acústicas.
El diseño del tubo se llevó a cabo mediante software de auto-CAD y para su análisis mecanoacústico utilizamos el método de los elementos finitos insertando el nuevo diseño en un modelo del oído medio ya desarrollado [5] por nuestro grupo.
Modelo 3D computadorizado basado en elementos finitos
El Método de los Elementos Finitos (FEM) es una herramienta numérica orientada a su implementación en computadoras utilizado en Ingeniería para predecir, en la fase de diseño, cómo se comportará el producto real ante alteraciones externas producidas por prácticamente cualquier fenómeno físico. El objetivo final del empleo de estos métodos es evitar, en lo posible, recurrir al costoso proceso, en tiempo y dinero, de construir prototipos y someterlos a ensayos, a veces destructivos, para comprobar que se comporta conforme a sus especificaciones en condiciones de trabajo.
Este método ya no considera la estructura como un continuo (como ocurría con los métodos clásicos de cálculo) sino que considera a cada sólido como un conjunto de pequeños elementos de dimensión finita relacionados entre sí a través de nodos o uniones de contacto. El comportamiento de cada uno de esos elementos se obtiene formulando un sistema de ecuaciones diferenciales y algebraicas. Las incógnitas serán los desplazamientos de los nodos, en función de los cuales expresaremos los desplazamientos de los puntos interiores de cada elemento formulando una hipótesis. Ensamblando los sistemas de ecuaciones se obtiene un sistema para todo el sólido con un elevado número de ecuaciones que puede ser resuelto con un ordenador.
Fundamentalmente, se trata de la resolución de la ecuación del movimiento:
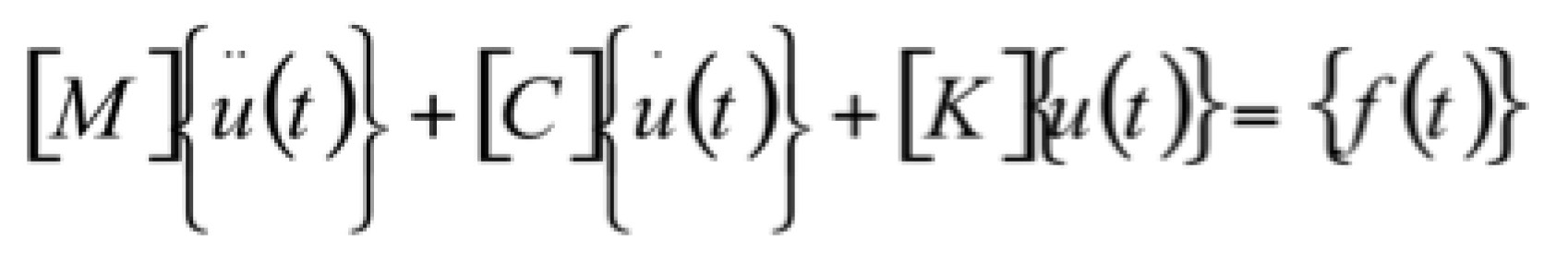
Donde: [M] = matriz de masa; [C] = matriz de amortiguamiento; [K] = matriz de rigidez; {u} = vector de desplazamientos; {f(t)} = vector de fuerzas
Las hipótesis que se van a plantear en el desarrollo del FEM son las siguientes:
• El medio continuo se divide en un número finito de elementos, cuyo comportamiento se define mediante un conjunto finito de parámetros o grados de libertad.
• Los elementos están conectados entre sí mediante un número discreto de puntos, que se denominan nodos, situados fundamentalmente en los contornos (aunque pueden existir nodos interiores). Los desplazamientos de los nodos son las variables incógnita del problema.
• El campo de desplazamientos dentro de cada elemento viene determinado por las funciones de forma, que los relaciona con los desplazamientos de los nodos de ese elemento. Es decir, el elemento se deforma, pero la deformación es conocida como función de los desplazamientos de sus nodos.
• Las funciones de forma se eligen por el usuario, cuando se crea el modelo, al elegir el tipo del elemento. Definen, de manera única, el campo de desplazamientos dentro de cada elemento finito, en función de los desplazamientos nodales de cada elemento.
• Se determina un sistema de fuerzas concentradas en los nodos, de forma que se equilibren las tensiones en el contorno y cualesquiera de las cargas repartidas.
Los pasos para realizar en el FEM son los siguientes:
1. Mallar la estructura en elementos finitos. Este paso me caracterizará el grado de confianza de los resultados obtenidos con posterioridad.
2. Formular la ecuación de comportamiento y determinar las propiedades de cada elemento, a partir de la geometría del problema, las propiedades del material, la naturaleza del problema los datos de cargas. Se escogerá el tipo de elemento finito más adecuado para resolver el problema.
3. Ensamblar las ecuaciones de cada elemento. Aplicación de las fuerzas y momentos exteriores.
4. Introducir las condiciones de contorno en la matriz ensamblada.
5. Resolver el sistema de ecuaciones y obtener la respuesta en tensiones o desplazamientos.
El modelo del oído humano simulado1 se obtuvo mediante el software Hypermesh 7.0 empleando los parámetros referenciados en la Tabla 1. La malla se exporta al software MSC Patran donde pre-procesamos, para posteriormente procesar en el software MSC Nastran. Una vez procesado el modelo, realizaremos nuevos ajustes en MSC Patran.
La validación del modelo simulado se realiza a través de la medida de la amplitud del desplazamiento del umbo. Para ello tomamos como referencia las medidas experimentales del desplazamiento del umbo realizada por Vlaming y Feenstra [6] y los resultados experimentales utilizando un vibrómetro láser monopunto en 4 voluntarios sanos a una intensidad sonora de 80 dB. Una vez que ya se conoce la curva de desplazamiento experimental, se puede validar el modelo simulado. Para ello, se calcula una función de respuesta en frecuencia que permite conocer el desplazamiento del umbo en el modelo simulado y comparar con los mediciones obtenidas experimentalmente [6].
Para la introducción de una prótesis en el modelo simulado del oído acoplado, ha de eliminarse los elementos que teóricamente serán reemplazados por la misma; en este caso, a pesar de no eliminarse, ya que solo se incide, ninguna porción de membrana, en el modelo procedimos a eliminar la superficie de la membrana timpánica que ocupará el tubo cuyo peso teórico es de 0,07 mg.
Para evaluar el comportamiento teórico de la nueva prótesis analizamos el desplazamiento, la impedancia y la función de transferencia (FT) en el modelo computadorizado del oído antes de ser manipulado y tras implantar el nuevo tubo en el mismo. La función de transferencia es la ganancia, o diferencia, de presión sonora medida entre dos puntos; Los puntos utilizados para calcular la función de transferencia fueron el umbo y un punto central de la platina.
Tabla 1. Parámetros empleados en la simulación computarizada del oído medio
|
Número de elemento |
NOMBRE |
DENSIDAD |
Módulo de Young (Pa) |
Coeficiente de Poisson |
Coeficiente |
|
1 |
Tejido biológico (membrana) |
1.200 |
3,30E+07 |
0,29 |
0,35 |
|
2 |
Músculo estapedial |
1.200 |
5,20E+05 |
0,2 |
0,2 |
|
3 |
Músculo tensor timpánico |
1.200 |
2,60E+06 |
0,2 |
0,2 |
|
4 |
Anillo timpánico |
500 |
2,10E+15 |
0,29 |
0,35 |
|
6 |
Ligamentos del yunque |
1.200 |
6,50E+05 |
0,29 |
0,3 |
|
7 |
Ligamento superior del martillo |
1.200 |
6,50E+05 |
0,3 |
0,25 |
|
8 |
Ligamento lateral del Martillo |
1.200 |
2,10E+07 |
0,3 |
0,25 |
|
9 |
Martillo (cuello) |
4.530 |
1,41E+10 |
0,2 |
0,05 |
|
10 |
Martillo (manubrio) |
3.700 |
1,41E+10 |
0,2 |
0,05 |
|
11 |
Martillo (cabeza) |
2.550 |
1,41E+10 |
0,2 |
0,05 |
|
12 |
Unión fibrosa tímpano-martillo |
50 |
2,00E+10 |
0,29 |
0,25 |
|
13 |
Articulación incudo-maleolar |
1.200 |
2,00E+10 |
0,4 |
0,25 |
|
14 |
Articulación incudo-estapedial |
1.200 |
7,00E+05 |
0,3 |
0,3 |
|
15 |
Apófisis corta del yunque |
2.260 |
1,41E+10 |
0,2 |
0,05 |
|
16 |
Cuerpo del yunque |
2.360 |
1,41E+10 |
0,2 |
0,05 |
|
17 |
Apófisis larga del yunque |
5.090 |
1,41E+10 |
0,2 |
0,05 |
|
18 |
Estribo |
2.200 |
1,41E+10 |
0,2 |
0,717 |
|
37 |
Timpano (fibras radiales) |
1.200 |
1,00E+07 |
0,3 |
0,35 |
|
38 |
Timpano (fibras parabólicas) |
1.200 |
1,00E+07 |
0,3 |
0,35 |
|
52 |
Timpano (fibras semilunares) |
1.200 |
1,00E+07 |
0,3 |
0,35 |
El tubo de equipresión transtimpánico (Patente Nº 201300509) está diseñado en silicona, material biocompatible con con los tejidos humanos. La geometría del mismo consta de un tubo, biselado en el que será el extremo medial del mismo, de diámetro externo de 1 mm y 0,8 mm de diámetro interno y de dos pares de alas flexibles (mediales y laterales) anguladas con respecto al eje del tubo de forma que se facilite su plegamiento durante la inserción y extracción del mismo (Figura 2A y B).
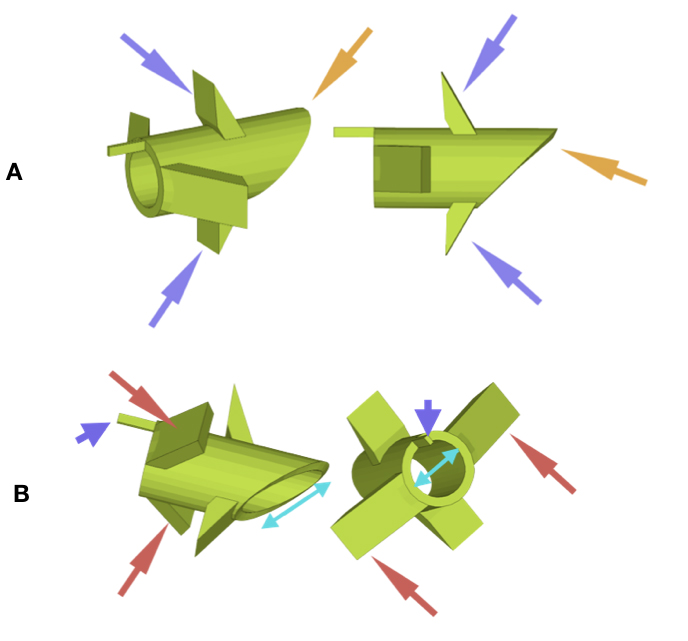
Figura 2. AExtremo medial del tubo biselado (flecha naranja) y alas internas flexibles (flechas moradas) que se pliegan al atravesar la membrana timpánica por la miringostomía practicada para desplegarse de nuevo en el oído medio una vez sobrepasada ésta. BProlongación lateral del tubo para permitir su agarre durante la extracción (Flecha morada) y alas laterales o externas (flechas rojas) que impiden la caída del tubo mientras está insertado y avisan al cirujano durante la colocación señalando el límite de profundidad de inserción al extenderse sobre el tímpano si se empuja en exceso.
La alas mediales se pliegan sobre el tubo al atravesar éste la membrana timpánica abriéndose de nuevo al sobrepasarla debido a su elasticidad; por el contrario, las alas laterales de mayor longitud que las mediales, si se sigue profundizando la inserción del tubo, se abren sobre la membrana timpánica evitando que el cirujano lo introduzca en exceso y caiga hacia la caja timpánica. Las alas mediales se sitúan entre sí a 180º (igual que las laterales). Entre sí ambos pares de alas se sitúan rotados 90º.
Una pequeña prolongación de silicona en el borde lateral del tubo facilita la prensión de este y su extracción.
Su peso teórico es de 0,75 mg (frente al tubo de Shepard de fluoroplástico de 12,44 mg y al de Goode en T corto de 6,79 mg)
El volumen relativo del nuevo diseño con respecto a los tubos de uso convencional de Shepard y de Goode se puede observar en la Figura 3. Al ser la masa y el volumen menor en el nuevo diseño su interferencia en la mecánica de la membrana timpánica se ve menos afectada. Cuando un elemento extraño es insertado en la membrana timpánica el modo de vibración de cada uno de estos elementos es distinto de forma que no vibran en fase (Figura 4) lo que induce tensiones en las fibras colágenas de la membrana. Esta característica es aún más manifiesta cuanto menor es la superficie de contacto entre membrana y tubo y mayor es la masa de éste. Como se puede ver en la Figura 5, las tensiones son máximas en determinados áreas de la membrana que, como se aprecia en la figura, coinciden con las zonas en las que se forman con más frecuencia placas de esclerosis en pacientes a los que se inserta un tubo de ventilación.
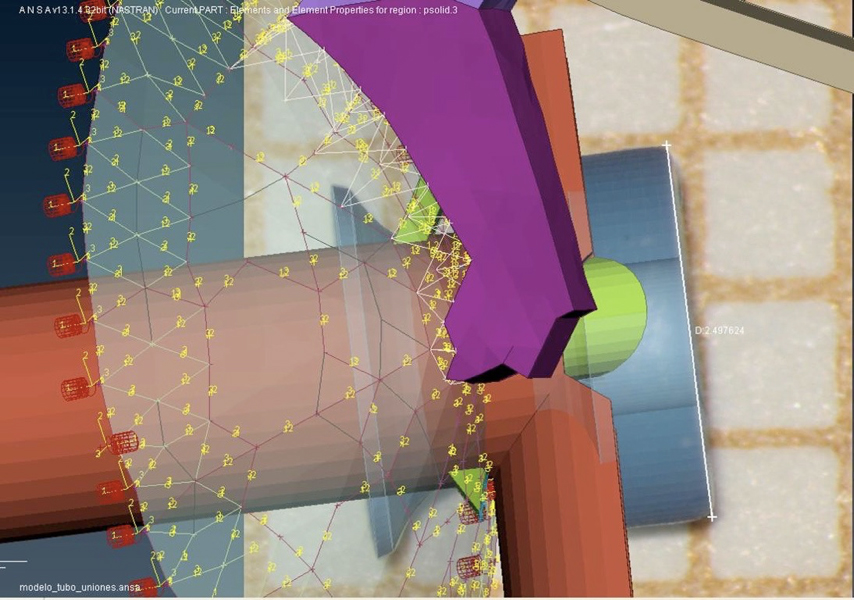
Figura 3. Superposición en el modelo computadorizado del nuevo tubo (verde) junto a los más frecuentemente utilizados: Shepard (azul) y Goode (rojo) todo ello sobre una malla milimetrada.
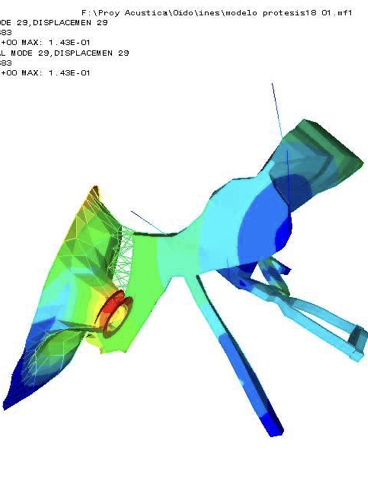
Figura 4. Imagen fija obtenida de una animación en el modelo computadorizado en el que se observa cómo la dinámica de la membrana timpánica se desacompasa enormemente con tubos de elevado peso como el modelado en esta imagen (tubo de titanio) haciendo que la vibración timpánica y la del tubo se desfasen. Este ausencia de vibración en fase puede ser la responsable, al originar tensiones en las fibras colágenas, de su degeneración y posterior aposición de depósitos cálcicos formando las placas de timpanosclerosis como complicación.
Otra consecuencia de una menor masa del diseño del nuevo tubo hace que su interferencia con la mecánica del oído medio sea menor; Así se puede cuantificar en el modelo computerizado 3D cómo los tubos de masa más elevada reducen el movimiento del umbo en un rango de frecuencias entre 600 y 3000 Hz, mientras que el comportamiento del nuevo tubo se superpone al del oído medio no modificado quirúrgicamente (Figura 6A); este mismo hecho también se pone de manifiesto cuando se analiza, en función de la frecuencia, el desplazamiento de un punto central de la platina (Figura 6B).
El diseño del nuevo tubo en silicona permite ser impregnado en óxido de plata a fin de reducir la formación de biofilms por St. aureus o Ps. aeruginosa con lo que es posible reducir, al menos teóricamnete, los episodios de otorrea.
La colocación de tubos transtimpánicos (también llamados de ventilación transtimpánicos, de timpanostomía o de equipresión) constituye el tratamiento de elección en pacientes con otitis seromucosa crónica con repercusión funcional [7] o en pacientes cuya membrana timpánica presente signos de sufrimiento [8].
Los tubos de equipresión transtimpánicos ayudan a ventilar el oído medio y, fundamentalmente, a equilibrar las presiones a cada lado de la membrana timpánica. Se han usado y usan, numerosos modelos de tubos de equipresión en el tratamiento de la otitis media seromucosa crónica: los de Shepard son los más usados en Europa, China y Sudáfrica y son eliminados de la membrana hacia los 6 meses tras su colocación [9]; por el contrario, el diseño de tubo de Armstrong es el preferido en América del Norte y se mantiene colocado en la membrana durante una media de 14 meses [10]. Por último, son los denominados tubos en T los que mayor durabilidad poseen no eliminándose por lo general espontáneamente [11]. A pesar de ello en un estudio de Hellström no se encuentran evidencias de una mejoría en la calidad de vida ni en la audición más allá de 9 meses tras la colocación de tubos de equipresión [12].
Otros estudios muestran que la mejoría en los umbrales auditivos tras colocar tubos de ventilación en de alrededor de 12 dB HL en los primeros tres meses [13-15] y no más de 5 dB de 6 a 9 meses tras su colocación [16,17] no habiéndose descrito evidencia alguna de su beneficio en cuanto a la inteligibilidad del lenguaje hablado o de un mayor desarrollo verbal en los niños que les portan [18].
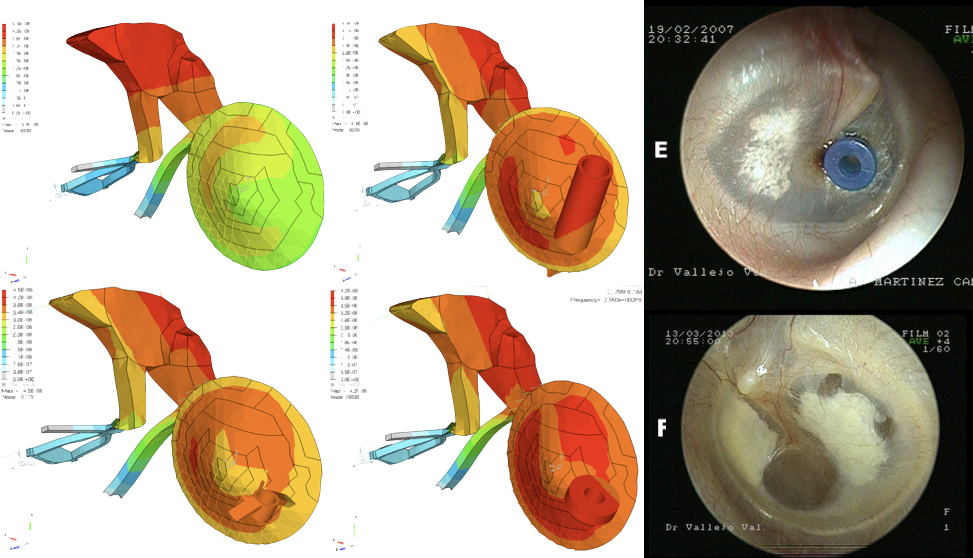
Figura 5. En las imágenes siguientes se muestran las tensiones teóricas soportadas al simular en el modelo computadorizado un estímulo sonoro de 1 kHz a 80 dB en un oído normal (A), en un oído con un tubo de Goode (B) o con el nuevo diseño (C) o con un tubo de Shepard (D); Las áreas de menor tensión se representan con colores fríos mientras que las de mayor tensión se marcan con colores tanto más cálidos cuanto mayor es la tensión. En las imágenes otoendoscópicas E y F se muestra la localización típica de las placas de timpanosclerosis tras portar tubos de miringostomía y su coincidencia con las áreas timpánicas que en el modelo soportan mayor tensión.
En cualquier caso, los tubos transtimpánicos constituyen una primera línea de tratamiento bajando su eficacia sea el parámetro que se estudie entre los 6 y 18 meses tras su colocación [9] siendo universalmente recomendados en niños con disfunción crónica de su trompa de Eustaquio. El riesgo de complicaciones es bajo; éstas aumentan su incidencia con los tubos en T en los que el lapso temporal medio que permanecen insertados es de 2 años de media [19]. La persistencia de anomalías en la membrana timpánica parece ser directamente proporcional al tiempo de permanencia timpánica de los tubos pero, aun así, no es posible determinar con seguridad si la responsabilidad en éstas es de los tubos o de la propia evolución de la enfermedad [20].
Los tubos de timpanostomía no previenen la progresión de la otitis media seromucosa hacia la atrofia timpánica y su impacto frente a la progresión hacia la formación de bolsas de retracción no ha sido bien determinada [21] pero sí parecen prevenir la formación de otitis media crónica colesteatomatosa [22].
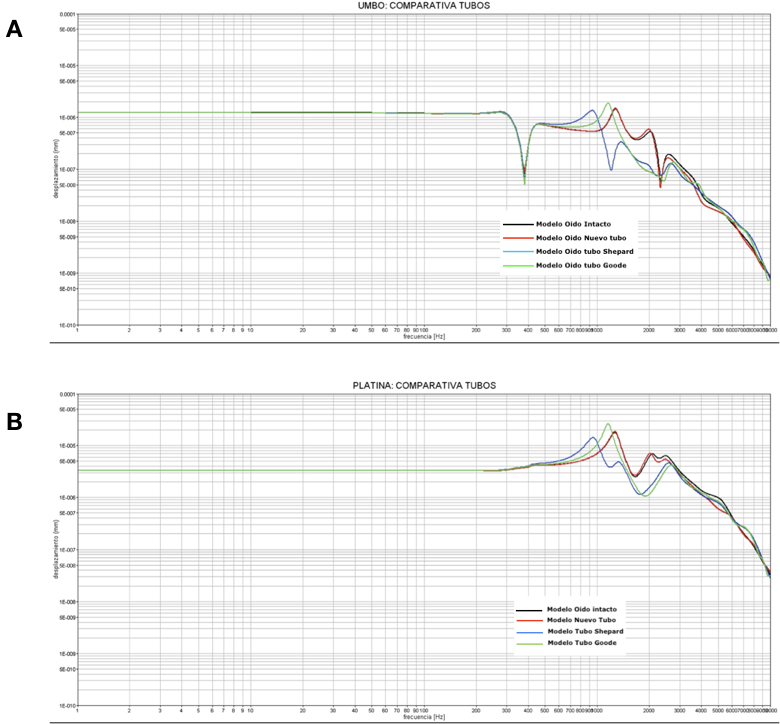
Figura 6. ARepresentación esquemática del movimiento del umbo timpánico en el modelo computadorizado al simular un estímulo de 80 dB de presión sonora: el trazado negro muestra, en un rango de frecuencias el desplazamiento del umbo de un oído no manipulado quirúrgicamente, el trazado rojo muestra el desplazamiento del umbo en un oído a donde se ha colocado un tubo de equipresión con el nuevo diseño; los trazados azul y verde muestran respectivamente el desplazamiento del umbo tras insertar un tubo de Shepard o uno de Goode. Nótense las distorsiones que sufre este movimiento entre las frecuencias 1 y 3 kHz en los supuestos de colocación de los tubos de Goode y Shepard, así como el comportamiento teórico casi superpuesto al del oído no manipulado quirúrgicamente en el caso del diseño del nuevo tubo. BComparativa similar a la anterior (y con las mismas condiciones y colores de los trazados) pero analizando en este caso el desplazamiento de un punto central en la platina del estribo. Nótense de nuevo en este gráfico las alteraciones teóricas que sufre el desplazamiento de la platina entre 1 y 2,5 kHz en oídos en los que se han insertado tubos de Shepard o Goode frente a aquel con el nuevo diseño de tubo.
Wallace y cols. [23] mostraron que la colocación de tubos de equipresión previene la recurrencia de la otitis seromucosa tras la caída o retirada de los mismos, estableciendo que el riesgo de padecer un episodio de otitis media seromucosa en niños que portaron tubos de equipresión es un 13% menor que en aquellos otros en los que la opción terapéutica fue la vigilancia o la paracentesis simple.
En niños con otitis seromucosa que presenten desórdenes del lenguaje o del aprendizaje se recomienda iniciar un tratamiento rápido de la misma a fin de limitar el impacto de una hipoacusia añadida. Esto es así en niños que padecen trastornos del espectro autista, hipoacusia neurosensorial añadida, retraso en el desarrollo del lenguaje, síndromes malformativos craneofaciales o con alteraciones visuales añadidas [24].
Las complicaciones tras la colocación de los tubos de equipresión son variables; así la otorrea oscila entre un 3 y un 50% de los casos en el postoperatorio inmediato siendo la más frecuente de las complicaciones asociadas a la colocación de tubos de ventilación; por lo general esta complicación es aislada y no suele dejar secuelas [25]. En la actualidad los tubos se impregnan en fábrica de preparados que dificultan o limitan la adhesión bacteriana a los mismos [26-29]. Sin embargo, otros autores no encuentran que los tubos así tratados químicamente presenten menos tasas de otorrea que los no tratados [30]. Es posible, entonces, pensar que esta complicación se deba al padecimiento de infecciones rinofaríngeas que, desde la trompa, alcanzan el oído medio por lo que la asociación de adenoidectomía a la implantación de los tubos reduce la incidencia de esta complicación.
Otras complicaciones descritas asociadas a la implantación de tubos de ventilación son la expulsión precoz, su obstrucción o la necesidad de remoción de los tubos por la alteración de la migración del epitelio timpánico pudiendo llegar a desarrollar la formación de colesteatoma de oído medio [31].
La incidencia de eliminación precoz se sitúa alrededor del 4%. Casi un 0.5% de los tubos caen hacia la cavidad timpánica [9]. La prevalencia de estas complicaciones depende del diseño del tubo, del nivel de experiencia del cirujano, y del tamaño de la miringotomía; Por el contrario, la larga permanencia del tubo (en T fundamentalmente) insertado en la membrana timpánica se asocia con mayores tasas de perforación residual; la prevalencia de esta complicación varía entre el 1 y 10% [31]. El diseño del tubo que presentamos en el trabajo evita la extrusión de este hasta que el otólogo considera que debe ser extraído, así como la caída hacia el oído medio.
La incidencia de obstrucción varía del 0% al 37% con una media próxima al 7% y consideramos que se debe más que al diseño del tubo o a su diámetro interno, a la persistencia de infecciones rinofaríngeas recurrentes que se extienden al oído medio desde la trompa por lo que abogamos por la realización de adenoidectomía sistemática asociada a la miringotomía. El diámetro interno del tubo que describimos es de 0,8mm, suficiente para equilibrar las presiones uno y otro lado de la membrana timpánica.
El desarrollo de miringosclerosis es otra secuela frecuente en tímpanos que alojaron tubos de ventilación; en la mayor parte de estos casos esta secuela carece de consecuencias clínicas, pero se han descrito casos de hipoacusia transmisiva por englobar el proceso timpanoscleroso parte de la cadena de huesecillos [31]. Diversos autores han señalado la importancia del diseño de los tubos de miringostomía en el desarrollo de placas de miringosclerosis [32,33,34]. Hemos visto, al implementar en un modelo computadorizado distintos diseños de tubos, que cuanto mayor es el peso de estos mayores son las discinesias observadas en la membrana timpánica y coincide que en estas áreas de mayores discinesias es donde más placas de esclerosis se forman; por esto pensamos que cuanto menor sea el peso del tubo de miringotomía menores serán estas áreas timpánica discinésicas y por tanto menores las posibilidades de formación de placas de miringosclerosis.
El diseño del tubo que mostramos en este trabajo cumple con los requisitos que Crysdale [4] estableció para el tubo ideal ya que:
• Su colocación es fácil al solo implicar enfrentar el extremo biselado del tubo a la miringotomía y empujarlo con suavidad para que se inserte si dificultad atravesando la membrana.
• El diseño de sus alas laterales o externas impide la caída hacia el oído medio
• Su eliminación no es espontánea como en los actuales, sino que su diseño facilita la remoción por el cirujano sólo cuando considere que las circunstancias patológicas que favorecen el padecimiento de la otitis seromucosa se han resuelto o mejorado.
• Dificulta el paso de agua u otros elementos hacia el oído medio al ser su diámetro interno menor que el de los tubos actuales.
• El material con el que está fabricado es tolerado perfectamente por la membrana timpánica al existir experiencia acumulada suficiente con los tubos actualmente comercializados y fabricados con este material.
• Puede cubrirse su superficie con preparados químicos que dificulten la formación de biofilms.
El nuevo diseño de tubo de miringostomía que presentamos resolvería algunos de los efectos indeseados que aparecen durante la utilización de los tubos de ventilación actualmente comercializados presentando algunas ventajas sobre ellos.
Ventajas biológicas porque el proceso de eliminación del tubo dejaría de ser imprevisible y dependería de la voluntad del médico pudiendo retirarse cuando las causas de disfunción tubárica hayan desaparecido o sea previsible un mejoría en su función y porque al poseer un menor tamaño que los actuales se evitan la formación de granulomas y placas de esclerosis.
Ventajas quirúrgicas debido a que el diseño biselado facilita su inserción favoreciendo la misma en situaciones complicadas como en oídos con atelectasias y a que se impide una introducción excesiva involuntaria y su caída (inmediata o diferida) hacia la caja timpánica. A las ventajas anteriores del nuevo diseño habría que añadir ventajas acústicas dado que su menor masa interfiere menos con la mecánica timpanoosicular lo que acarrearía menores consecuencias funcionales sobre el oído en el que se implanta.
1. Bray D, Owa A. How we do it: OWA (Addengrookes) grommet. Clin Otolaryngol. 2006;31:62-3.
2. D’Eredita R, Marsh RR. Tympanic membrane healing process and biocompatibility of an innovative absorbable ventilation tube. Otol Neurotol 2006;7:65-70.
3. Park AH, Hoyt D, Britt D, Chase S, Transavatdi K, Hunter L, Sheng X, Prestwich GD. Cross-linked hydrogel and polyester reservable ventilation tubes in chinchilla model. Laryngoscope 2013;123:1043-8.
4. Crysdale WS. Comparative study of various ventilating tubes. Ann Otol Rhinol. Laryngol. 1976;85:268-9.
5. Gil-Carcedo E, Pérez-López B, Vallejo LA, Gil-Carcedo LM, Montoya F. Modelo Computadorizado 3-D para el estudio de la biomecánica del oído medio con el Método de los Elementos Finitos (MEF) Acta Otorrinolaringológica Española 2002;53: 527-37.
6. Vlaming MSMG, Feenstra L. Studies on the mechanics of the normal human middle ear. Clinical Otolaryngology 1986;11:353-63.
7. Ito M, Takahashi H, Iino Y, et al. Clinical practice guidelines for the diagnosis and management of otitis media with effusion (OME) in children in Japan, 2015. Auris Nasus Larynx. 2017;44(5):501-8.
8. Simon F, Haggard M, Rosenfeld RM, et al. International consensus (ICON) on management of otitis media with effusion in children. Eur Ann Otorhinolaryngol Head Neck Dis. 2018;135(1S):S33-S39.
9. Vanneste P, Page C. Otitis media with effusion in children: Pathophysiology, diagnosis, and treatment. A review. J Otol. 2019;14(2):33-9.
10. Rosenfeld RM, Schwartz SR, Pynnonen MA, et al. Clinical practice guideline: Tympanostomy tubes in children. Otolaryngol Head Neck Surg. 2013;149(1 Suppl):S1-S35.
11. Söderman AC, Knutsson J, Priwin C, von Unge M. A randomized study of four different types of tympanostomy ventilation tubes One-year follow-up. Int J Pediatr Otorhinolaryngol. 2016;89:159-63.
12. Hellström S, Groth A, Jörgensen F, Pettersson A, Ryding M, Uhlén I, Boström KB. Ventilation tube treatment: a systematic review of the literature. Otolaryngol Head Neck Surg. 2011;145:383-95.
13. Fergie N, Bayston R, Pearson JP, Birchall JP. Is otitis media with effusion a biofilm infection?. Clin Otolaryngol Allied Sci. 2004;29(1):38-46.
14. Hall-Stoodley L, Hu FZ, Gieseke A, et al. Direct detection of bacterial biofilms on the middle-ear mucosa of children with chronic otitis media. JAMA. 2006;296(2):202-11.
15. Van Hoecke H, De Paepe AS, Lambert E, et al. Haemophilus influenzae biofilm formation in chronic otitis media with effusion. Eur Arch Otorhinolaryngol. 2016;273(11):3553-60.
16. Blanc F, Ayache D, Calmels MN, et al. Management of otitis media with effusion in children. Société française d’ORL et de chirurgie cervico-faciale clinical practice guidelines. Eur Ann Otorhinolaryngol Head Neck Dis. 2018;135(4):269-73.
17. Maris M, Wojciechowski M, Van de Heyning P, Boudewyns A. A crosssectional analysis of otitis media with effusion in children with Down syndrome. Eur J Pediatr. 2014;173(10):1319-25.
18. Browning GG, Rovers MM, Williamson I, Lous J, Burton MJ. Grommets (ventilation tubes) for hearing loss associated with otitis media with effusion in children. Cochrane Database Syst Rev. 2010;(10):CD001801.
19. Lindstrom DR, Reuben B, Jacobson K, Flanary VA, Kerschner JE. Long-term results of Armstrong beveled grommet tympanostomy tubes in children. Laryngoscope. 2004;114(3):490-4.
20. De Beer BA, Schilder AG, Zielhuis GA, Graamans K. Natural course of tympanic membrane pathology related to otitis media and ventilation tubes between ages 8 and 18 years. Otol Neurotol. 2005;26(5):1016-21.
21. Johnston LC, Feldman HM, Paradise JL, et al. Tympanic membrane abnormalities and hearing levels at the ages of 5 and 6 years in relation to persistent otitis media and tympanostomy tube insertion in the first 3 years of life: a prospective study incorporating a randomized clinical trial. Pediatrics. 2004;114(1):e58-e67.
22. Djurhuus BD, Christensen K, Skytthe A, Faber CE. The impact of ventilation tubes in otitis media on the risk of cholesteatoma on a national level. Int J Pediatr Otorhinolaryngol. 2015;79(4):605-9.
23. Wallace IF, Berkman ND, Lohr KN, Harrison MF, Kimple AJ, Steiner MJ. Surgical treatments for otitis media with effusion: a systematic review. Pediatrics. 2014;133(2):296-311.
24. Rosenfeld RM, Shin JJ, Schwartz SR, et al. Clinical Practice Guideline: Otitis Media with Effusion (Update). Otolaryngol Head Neck Surg. 2016;154(1 Suppl):S1-S41.
25. Vlastarakos PV, Nikolopoulos TP, Korres S, Tavoulari E, Tzagaroulakis A, Ferekidis E. Grommets in otitis media with effusion: the most frequent operation in children. But is it associated with significant complications?. Eur J Pediatr. 2007;166(5):385-91.
26. Antonelli PJ, Sampson EM, Ojano-Dirain C. Biofilm formation on silicone tympanostomy tubes with polyvinylpyrrolidone coating. Arch Otolaryngol Head Neck Surg. 2011;137(1):19-23.
27. Jang CH, Cho YB, Choi CH. Effect of ionbombarded silicone tympanostomy tube on ciprofloxacin-resistant Pseudomonas aeruginosa biofilm formation. Int J Pediatr Otorhinolaryngol. 2012;76(10):1471-3.
28. Saidi IS, Biedlingmaier JF, Whelan P. In vivo resistance to bacterial biofilm formation on tympanostomy tubes as a function of tube material. Otolaryngol Head Neck Surg. 1999;120(5):621-7.
29. Wang JC, Tran PL, Hanes R, et al. Inhibition of otopathogenic biofilms by organoselenium-coated tympanostomy tubes. JAMA Otolaryngol Head Neck Surg. 2013;139(10):1009-16.
30. Hong P, Smith N, Johnson LB, Corsten G. A randomized double-blind controlled trial of phosphorylcholine-coated tympanostomy tube versus standard tympanostomy tube in children with recurrent acute and chronic otitis media. Laryngoscope. 2011;121(1):214-9.
31. Kay DJ, Nelson M, Rosenfeld RM. Metaanalysis of tympanostomy tube sequelae. Otolaryngol Head Neck Surg. 2001;124(4):374-80.
32. Dingle AF, Flood LM, Kumar BU, Newcombe RC. Tympanosclerosis and mini grommets: the relevance of grommet design. J Laryngol Otol. 1995;109(10):922-5.
33. Kazikdas KC, Serbetcioglu B, Boyraz I, et al. Tympanometric changes in an experimental myringosclerosis model after myringotomy. Otol Neurotol. 2006;27(3):303-7.
34. Prendergast PJ; Kelly DJ; Rafferty M, Blayney AW. The effect of ventilation tubes on stresses and vibration motion in the tympanic membrane: a finite element analysis. Clin Otolaryngol Allied Sci. 1999;24:542-8.